- 029-86354885
- 18392009562
脂質(zhì)體藥物用于腫瘤臨床已逾20余年,然而臨床抗腫瘤療效并不理想,原因有:在脂質(zhì)體系統(tǒng)到達(dá)腫瘤部位之前,裝載的藥物在循環(huán)系統(tǒng)中發(fā)生泄漏,導(dǎo)致腫瘤部位的藥物暴露量減少,同時(shí)也增加了對(duì)健康器官的損害。藥物泄漏由血漿蛋白等引起,這些蛋白破壞脂質(zhì)體雙層的完整性。同時(shí)還有血流剪切力增加脂質(zhì)體膜的形變和滲透性,導(dǎo)致藥物泄漏等。
許多因素影響脂質(zhì)體的穩(wěn)定性,如磷脂類型和組成比、藥脂比、膽固醇含量等。聚合物表面修飾是提高脂質(zhì)體穩(wěn)定性的重要方法,聚合物(通常為PEG)可以與脂質(zhì)的頭部基團(tuán)共價(jià)連接,或物理吸附在脂質(zhì)體的外表面,以排斥血清蛋白的吸附并調(diào)節(jié)藥物的釋放。聚合物還可通過交聯(lián)形成籠狀的保護(hù)層。也有研究建立了納米粒穩(wěn)定的脂質(zhì)體,帶電納米粒子在磷脂雙層膜上的非特異性吸附可提供空間和靜電排斥力,進(jìn)而防止脂質(zhì)體相互融合。已有的方法大多數(shù)是修飾脂質(zhì)體表面,這可能同時(shí)引入不利的納米-生物界面相互作用,有必要開發(fā)一種新的保持脂質(zhì)體的表面特性不變的新的穩(wěn)定化方法。
納米碗嵌入脂質(zhì)體內(nèi)水腔,創(chuàng)建了一種納米碗支撐的脂質(zhì)體(NbLipo),該系統(tǒng)可顯著增強(qiáng)藥物(阿霉素DOX)的裝載(DOX@NbLipo ),并有效抵抗血清蛋白和血流剪切力導(dǎo)致的藥物泄露。
其主要原理和機(jī)制如下:
(1)納米碗開口角為90-110°(開口面積占內(nèi)水腔表面積的14.6-21.3%),與普通脂質(zhì)體相比,減少了藥物從內(nèi)水腔中泄漏的面積。
( 2)納米碗為剛性結(jié)構(gòu),其對(duì)脂質(zhì)體雙分子層的支撐作用(楊氐模量NbLipo為2.6MPa,為普通脂質(zhì)體( 0.08 MPa )的32.5倍)可抵抗血清或血流剪切力對(duì)膜結(jié)構(gòu)的破壞。
(3)剛性納米碗可以抵抗硫酸阿霉素晶體對(duì)脂質(zhì)體雙層的破壞(導(dǎo)致包封率降低),并在高藥脂比(0.5)時(shí)仍獲得高效裝載(包封率>95%)。
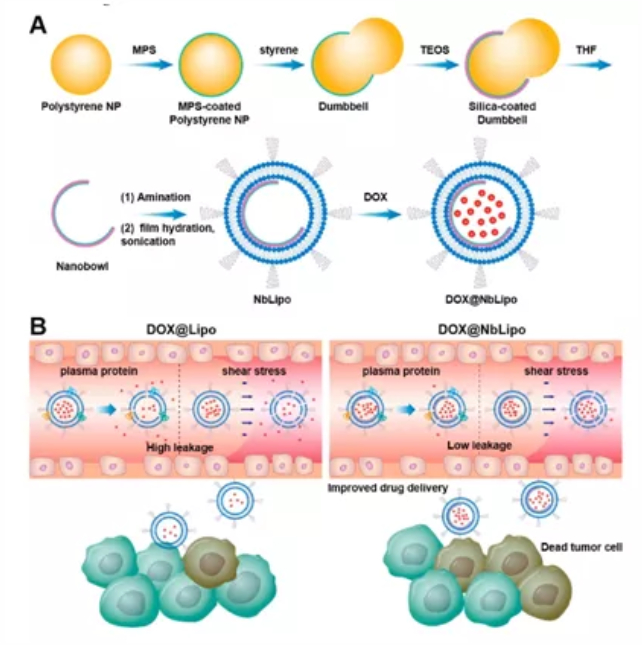
研究表明,攝取進(jìn)入腫瘤細(xì)胞后,DOX@NbLipo中的藥物仍可獲得快速、高效釋放。與普通阿霉素脂質(zhì)體(DOx@Lipo )相比,DOX@NbLipo具有更長的血漿半衰期,可將更多的藥物DOX遞送至4T1原位乳腺腫瘤部位,顯著抑制腫瘤生長和肺轉(zhuǎn)移,與未處理組(生理鹽水組)相比,DOX@NbLipo治療組中位生存期(50天)延長率達(dá)108.3%。
| 序號(hào) | 新聞標(biāo)題 | 瀏覽次數(shù) | 作者 | 發(fā)布時(shí)間 |
|---|---|---|---|---|
| 1 | 抗氧化小分子70831-56-0,菊苣酸Cichoric Acid,6537-80-0的制備過程 | 752 | 瑞禧生物 | 2023-03-30 |
| 2 | 活性氧ROS小分子Dapsone,cas:80-08-0,氨苯砜的制備過程-瑞禧科研 | 668 | 瑞禧生物 | 2023-03-30 |
| 3 | HBPS-N3,Azide-PEG-HBPS,疊氮化超支化聚苯乙烯高分子聚合物的制備過程 | 780 | 瑞禧生物 | 2023-03-17 |
| 4 | l-PS-PhN3,Azide疊氮Azido偶聯(lián)線性聚苯乙烯雙鏈的制備過程 | 724 | 瑞禧生物 | 2023-03-17 |
| 5 | N3-PS-N3,Azido-PS-Azido/Azide,雙疊氮官能團(tuán)修飾聚苯乙烯的制備方法 | 683 | 瑞禧生物 | 2023-03-17 |
| 6 | PS-N3,Azido-PS,疊氮Azide修飾聚苯乙烯/高分子聚合物的制備過程 | 853 | 瑞禧生物 | 2023-03-17 |
| 7 | Azido-PEG2-t-Butylester/1271728-79-0,疊氮N3/ZAD修飾叔丁酯化合物的制備方法 | 699 | 瑞禧生物 | 2023-03-14 |

 400-115-0588
400-115-0588 在線咨詢
在線咨詢







 庫存查詢
庫存查詢